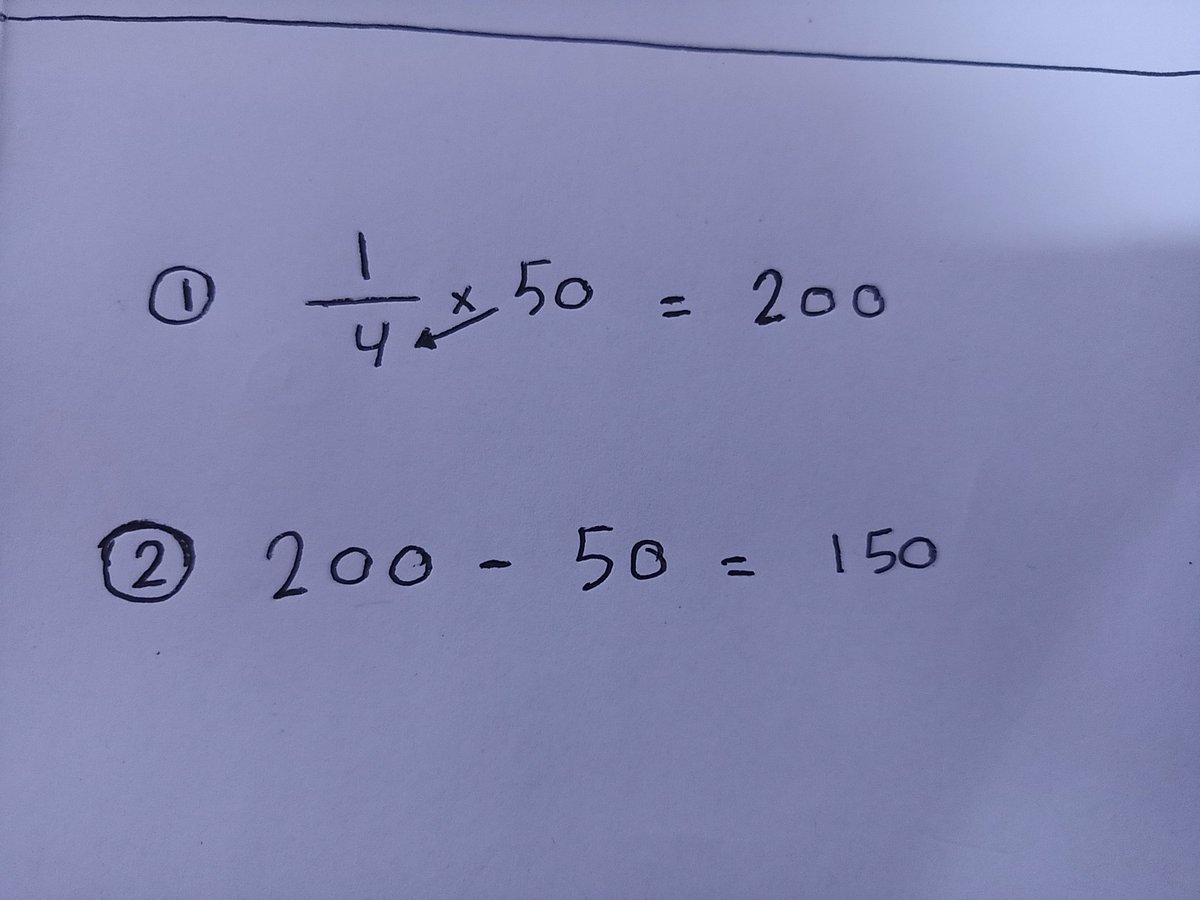السلام عليكم 👋🏻
** مهم جدا لفني/ة المختبر معرفة كل شيء عن التخفيف.. 🤓
أولا: ما هو التخفيف أو Dilution 🤔؟
هو عبارة عن عمل نقوم به للتقليل من تركيز العينة باستخدام diluent.
يتبع..
#أحلام_راضي
** مهم جدا لفني/ة المختبر معرفة كل شيء عن التخفيف.. 🤓
أولا: ما هو التخفيف أو Dilution 🤔؟
هو عبارة عن عمل نقوم به للتقليل من تركيز العينة باستخدام diluent.
يتبع..
#أحلام_راضي
*نعرف Diluent من خلال البامفلت.. وقد يكون:
1. Normal saline (وهو الأكثر شيوعاً).
2. أو Distilled water.
1. Normal saline (وهو الأكثر شيوعاً).
2. أو Distilled water.
ثانياً: لماذا احتاج إلى عمل تخفيف بالمختبر 🤔؟
هو أن كل جهاز يقدر يقيس تركيز مادة إلى حد معين ( وهذا ما يسمى بال Linearity limit ) وهو أعلى تركيز ممكن يقيسه الجهاز، اما اذا تجاوزت النتيجة هذا الحد، إذن احتاج إلى عمل تخفيف للعينة للوصول الى التركيز الصحيح بدقة.
هو أن كل جهاز يقدر يقيس تركيز مادة إلى حد معين ( وهذا ما يسمى بال Linearity limit ) وهو أعلى تركيز ممكن يقيسه الجهاز، اما اذا تجاوزت النتيجة هذا الحد، إذن احتاج إلى عمل تخفيف للعينة للوصول الى التركيز الصحيح بدقة.
* نعرف Linearity limit أيضاً من خلال البامفلت.
ثالثاً: انواع التخفيف 🤓
1. Simple dilution.
- يكون في خطوة واحدة.
- يكون في clinical chemistry test 🧪.
2. Serial dilution
- يكون عدة خطوات.
- يكون في serological test مثل فحص CRP.
1. Simple dilution.
- يكون في خطوة واحدة.
- يكون في clinical chemistry test 🧪.
2. Serial dilution
- يكون عدة خطوات.
- يكون في serological test مثل فحص CRP.
🟢نركز الان على Simple dilution 🟢
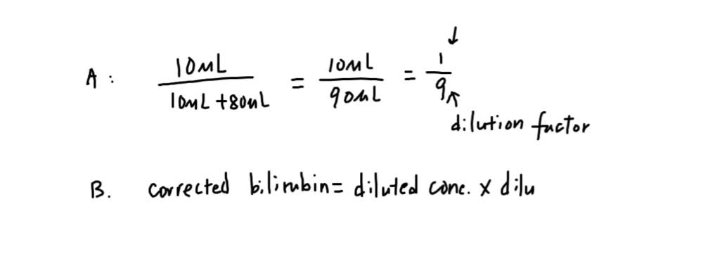
قانون التخفيف = حجم العينة/ الحجم الكلي.
*الحجم الكلي: عبارة عن حجم العينة + حجم مادة التخفيف
قانون التخفيف = حجم العينة/ الحجم الكلي.
*الحجم الكلي: عبارة عن حجم العينة + حجم مادة التخفيف
نطبقها على قانون التخفيف= 50/ (50+150)
=50/200
= 1/4
=50/200
= 1/4
*مثال ثاني سريع: نأخذ من العينة 10 مايكرو ونريد التخفيف 1/3.
الحل: 👇🏻
10×3= 30
30-10=20
*إذن ساخذ diluent 20
تطبيق على القانون=10/(10+20)
=1/3
الحل: 👇🏻
10×3= 30
30-10=20
*إذن ساخذ diluent 20
تطبيق على القانون=10/(10+20)
=1/3
* نعرف كم التخفيف المطلوب أيضا من خلال البامفلت.
شكراً لكل شخص وصل لحد هنا 🌹🌹 أرحب جدا بالأسئلة 😃🙃.
جاري تحميل الاقتراحات...