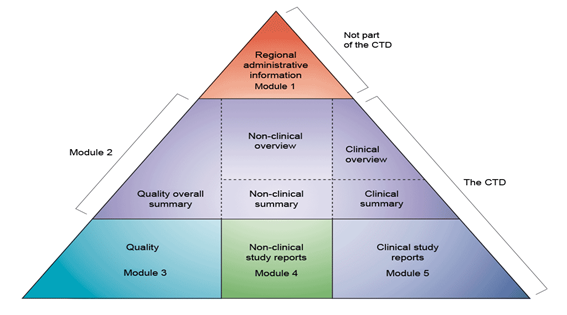
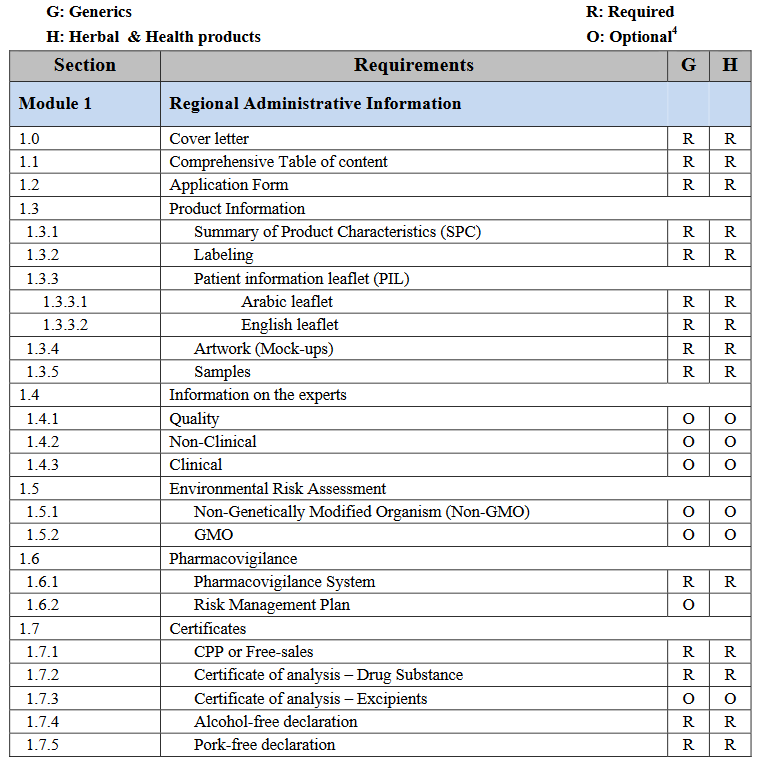
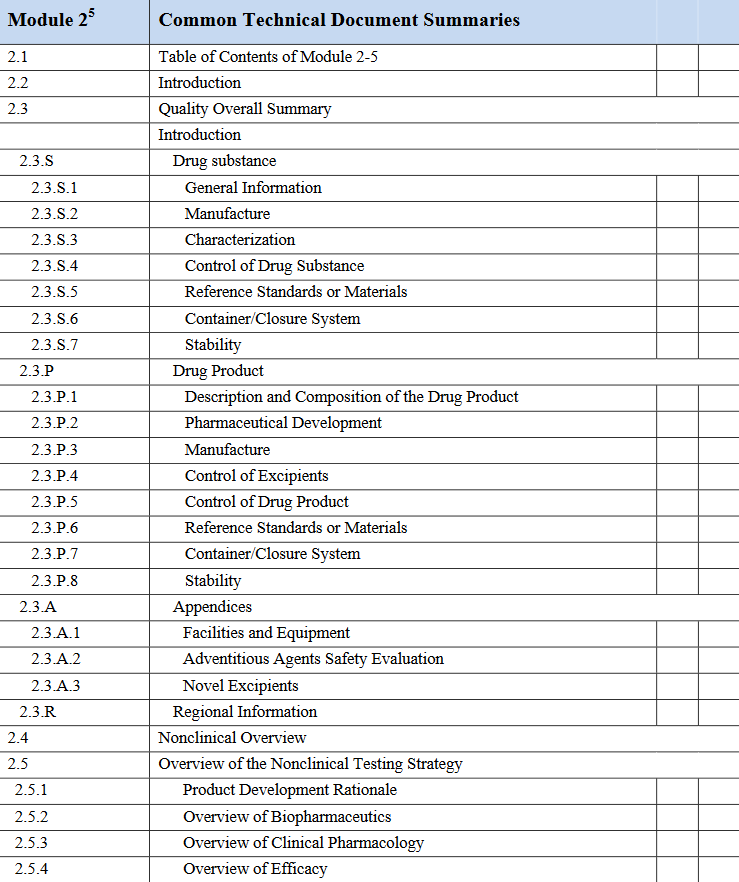
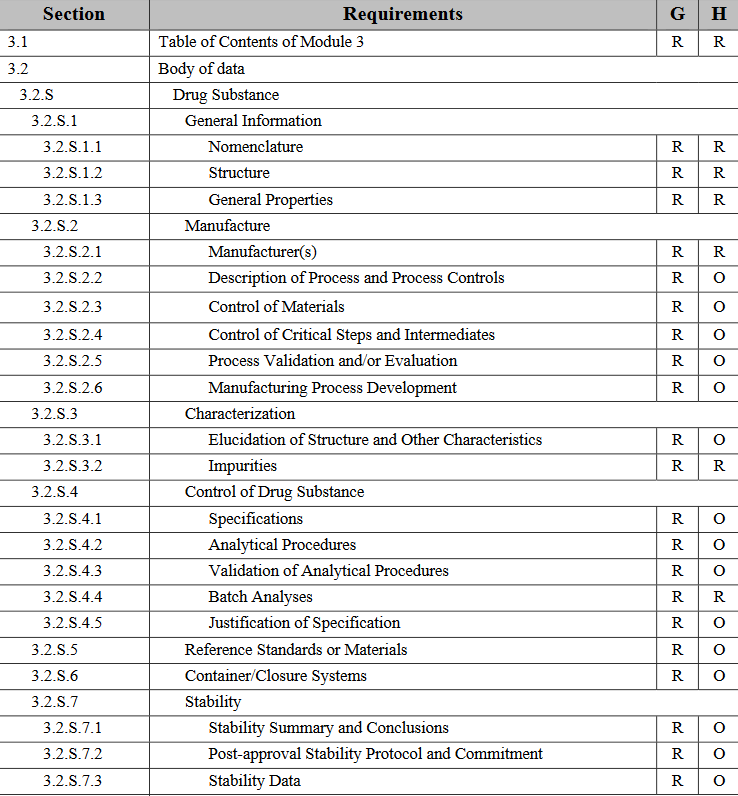
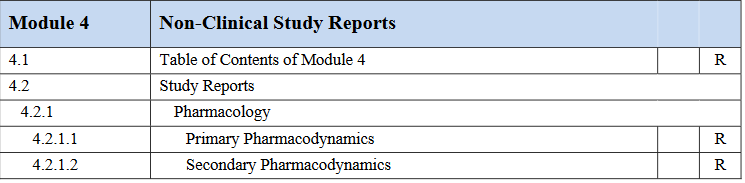
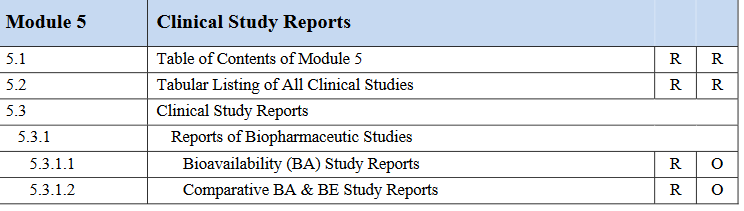
الهدف من اتباع الصيغة الموحدة (eCTD) ؟
توحيد المتطلبات و طبيعة المعلومات الفنية الواجب توفرها في ملفات التسجيل لضمان جودة وفعالية و مأمونية المستحضرات المراد تطويرها.
توحيد المتطلبات و طبيعة المعلومات الفنية الواجب توفرها في ملفات التسجيل لضمان جودة وفعالية و مأمونية المستحضرات المراد تطويرها.
جاري تحميل الاقتراحات...